內分泌與代謝病學科文獻學習系列活動
在目前的基礎研究領域中,cGAS-STING pathway正成為一個越來越熱門的研究方向。2023年11月1日,內分泌與代謝病學科第148期文獻學習系列活動特邀同濟大學附屬上海市肺科醫院劉海鵬研究員,為內分泌科師生開展學術講座——基于cGAS-STING信號通路的腫瘤靶向干預研究。

劉海鵬研究員及其團隊多年來致力于肺部腫瘤與肺部感染的基礎和轉化研究,以固有免疫分子為切入點,致力于疾病靶標的發現和干預。近年來聚焦于cGAS-STING信號通路,系統闡述了cGAS的多種新型生物學功能及其調控機制,為靶向調控cGAS-STING通路治療腫瘤和自身免疫性疾病等的臨床應用及藥物開發提供了重要的理論基礎。相關研究結果以第一或通訊作者發表在Nature、Molecular Cell、Nature Communication、Autophagy、EMBO Reports等雜志。授權發明專利4項,參與項目獲得教育部自然科學一等獎1項。研究獲得國家自然科學基金(5項)、上海市科委、上海市教委等項目資助。
劉海鵬教授首先通過簡要介紹免疫反應的基礎知識展開了今天的文獻學習活動,闡述了免疫反應和肺部疾病(尤其是肺部腫瘤)的關系。
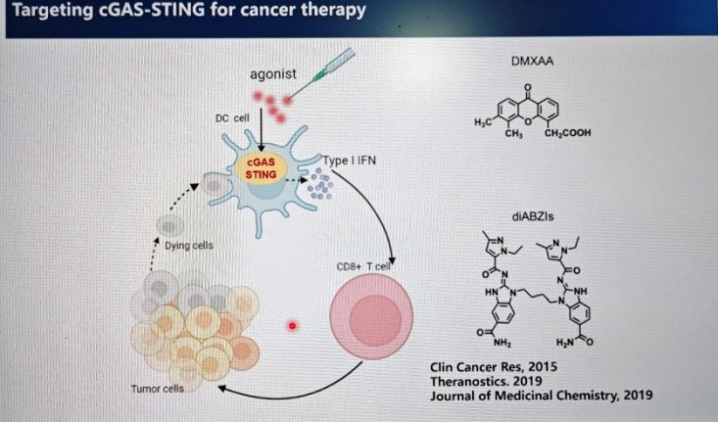
劉教授介紹了cGAS-STING pathway具體通路上的各個分子和反應,包括cGAS的概念、作用以及在不同領域、不同方面所擔任的重要角色。
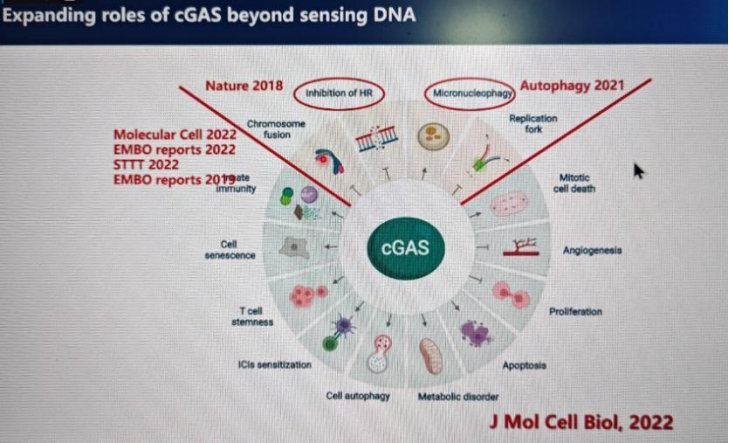
?
接下來,劉教授介紹了cGAS-STING pathway的經典代謝過程研究。劉教授以鉑類藥物在肺癌治療中的化療抵抗為問題,展開了研究的全面講解。在基礎研究中,劉教授團隊發現,cGAS-STING pathway會誘導1型干擾素的生成,從而改善鉑類藥物引起的化療抵抗。這一發現給我們在臨床上制定不同的肺癌化療方案帶來了啟發,Bricanib和platinum結合治療有望在未來的肺癌治療中發揮重要作用。在上述研究中,劉教授團隊系統闡述了cGAS的多種生物學功能及其調控機制,開發了靶向cGAS-STING信號通路的新的小分子藥物,為靶向調控cGAS-STING通路治療腫瘤和自身免疫性疾病等的臨床應用及藥物開發提供了重要的理論基礎。
另一方面,STING的翻譯后修飾目前已有較多研究,劉教授對STING從ER出去的精細過程作了簡要介紹。研究發現,STING的活化是TAK1活化所必須的,同時,TAK1對STING的活化也是非常重要且不可或缺的。劉教授團隊針對STING和TAK1之間如何互相活化及其相關關系開展基礎研究,在講解中將STING離開ER的過程比喻成船離開碼頭的過程,生動形象地介紹了STING和TAK1之間的相互關系。
隨后,劉教授耐心地解答了陳燕銘教授、石國軍主任、朱延華主任、徐芬研究員等老師及各位同學的疑問。
最后,在學科帶頭人陳燕銘教授的總結中,本次文獻學習活動圓滿落下帷幕。









